4.2.3 Endoxidation (aerobe Atmungskette): Unterschied zwischen den Versionen
| (Eine dazwischenliegende Version desselben Benutzers wird nicht angezeigt) | |||
| Zeile 1: | Zeile 1: | ||
| − | Die '''Endoxidation''' findet | + | Die '''Endoxidation''' findet stets ans Membranstrukturen statt. Bei eukaryontischen '''Dissimilierern''' ist das die innere Mitochondrienmembran, cytoplasmatische Membranstrukturen bei Prokaryonten. |
Von den H-beladenen Coenzymen werden die H-Atome an der Membran über eine Kette von Überträgerproteinen bis zum O<sub>2</sub> transportiert (ab den Cytochromen zunächst nur die Elektronen). Dort kommt es zunächst zur Reaktion der Elektronen: | Von den H-beladenen Coenzymen werden die H-Atome an der Membran über eine Kette von Überträgerproteinen bis zum O<sub>2</sub> transportiert (ab den Cytochromen zunächst nur die Elektronen). Dort kommt es zunächst zur Reaktion der Elektronen: | ||
| − | <div align=center>0,5O<sub>2</sub> + 2e<sup>-</sup> → | + | <div align=center>0,5O<sub>2</sub> + 2e<sup>-</sup> → O<sup>2-</sup> (Oxid-Ion)</div> |
bzw. | bzw. | ||
| − | <div align=center> | + | <div align=center>O<sup>2</sup> + 4e<sup>-</sup> → 2O<sup>2-</sup>.</div> |
Die Elektronen stammen aus 1 bzw. 2 NADH/H<sup>+</sup>. Die Oxid-Ionen reagieren mit den Protonen in der biologischen Knallgasreaktion zu Wasser: | Die Elektronen stammen aus 1 bzw. 2 NADH/H<sup>+</sup>. Die Oxid-Ionen reagieren mit den Protonen in der biologischen Knallgasreaktion zu Wasser: | ||
<div align=center>2O<sup>2-</sup> + 4H<sup>+</sup> → 2H<sub>2</sub>O</div> | <div align=center>2O<sup>2-</sup> + 4H<sup>+</sup> → 2H<sub>2</sub>O</div> | ||
Aktuelle Version vom 3. März 2010, 11:21 Uhr
Die Endoxidation findet stets ans Membranstrukturen statt. Bei eukaryontischen Dissimilierern ist das die innere Mitochondrienmembran, cytoplasmatische Membranstrukturen bei Prokaryonten. Von den H-beladenen Coenzymen werden die H-Atome an der Membran über eine Kette von Überträgerproteinen bis zum O2 transportiert (ab den Cytochromen zunächst nur die Elektronen). Dort kommt es zunächst zur Reaktion der Elektronen:
bzw.
Die Elektronen stammen aus 1 bzw. 2 NADH/H+. Die Oxid-Ionen reagieren mit den Protonen in der biologischen Knallgasreaktion zu Wasser:
Die hierbei benötigten H+-Ionen stammen ebenfalls aus NADH/H+. Pro O2-Molekül müssen also 4 H-Atome die Atmungskette durchlaufen. Es können während der Atmungkette folgende Schritte differenziert werden:
- 1. Schritt:
- NADH/H+ + Flavoprotein → H-beladenes Flavoprotein + NAD+ + ATP
- 2. Schritt:
- H-beladenes Flavoprotein + Q[1] → QH2[2] + Flavoprotein
Die nun folgenden Überträgerproteine heißen Cytochrome. Ab ihnen werden nur noch Elektronen übertragen. Die H+ bleiben gelöst. Jedes Cytochrommolekül hat ein zentrales Fe3+-Ion, das nur 1e- aufnehmen kann. Daher werden immer zwei Cytochrommoleküle für jeden Übertragungsschritt benötigt.
- 3. Schritt:
- QH2 + 2 Cytochrom b (2Fe3+) → Q + 2H+ + 2 Cytochrom b (Fe2+)
- 4. Schritt:
- 2 Cytochrom b (2Fe2+) + 2 Cytochrom c (2Fe3+) → 2 Cytochrom b (2Fe3+) + 2 Cytochrom c (2Fe2+)
- 5. Schritt:
- 2 Cytochrom b (2Fe2+) + Cytochromoxidase (2Fe3+) → 2Cytochrom c (2Fe3+) + Cytochromoxidase (Fe2+) + ATP
- 6. Schritt:
- Cytochromoxidase (2Fe3+) + 0,5O2 → Cytochromoxidase (2Fe3+) + O2- + ATP
- 7. Schritt:
- O2- + 2H+ → H2O
Organismen, die diesen Weg der Energiegewinnung durchführen, betreiben Dissimilation oder Zellatmung. Sie ist also die Umwandlung von (i. d. R.) Glucose und Sauerstoff zu Wasser und Kohlenstoffdioxid:
Dissimilierer sind z. B. Bakterien, einzellige Tiere und Pflanzen (sie betreiben sowohl Dissimilation als auch Assimilation bzw. Photosynthese).
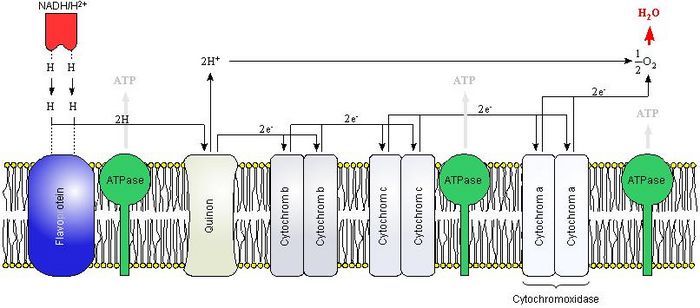
Abb. 25: Endoxidation bei der aeroben Atmungskette
[1]: Quinon
[2]: Hydroquinon